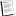
Αυτό που ισχύει σαν κανόνας για τη διάλυση του CaCO3 στο νερό, γενικά ακολουθεί τον εξής απλό κανόνα:
α) Αύξηση παροχής CO2 στο σύστημα, μείωση διαλυτότητας [Ca++] => δημιουργία ιζήματος. (Φυσικά ισχύει κ το ανάστροφο)
β) Αύξηση αλατότητας (salinity) υπό σταθερή θερμοκρασία κ pH => αύξηση διαλυτότητας [Ca++]. (λειτουργεί ανάστροφα)
γ) Αύξηση θερμοκρασίας, υπο σταθερό pH => μείωση διαλυτότητας [Ca++].
δ) Αύξηση Ph => δραστική μείωση της διαλυτότητας του ασβεστόλιθου. Με pH>8 η διαλυτότητά του είναι σχεδόν αμελητέα στο γλυκό νερό. Με ελαφρά αύξηση της αλατότητας, ελαφρά αύξηση της διαλυτότητας του CaCO3, (δλδ σε θαλασσινά ενυδρεία).
Επίσης η διαλυτότητας οποιασδήποτε ουσίας ναι επηρεάζεται από την επιφάνεια του υλικού το οποία είναι προς διάλυση. Έτσι αύξηση κοκκομετρίας κ πορώδους, συνεπάγεται αύξηση επιφάνειας, άρα και αύξηση διαλυτότητας. Η ροή ναι ενδεχομένως να λειτουργεί θετικά στην διάλυση του ασβεστόλιθου.
Τα σαλιγκάρια εφόσον έχουν ασβεστολιθικά καβούκια, προφανώς συμμετέχουν κατά ένα μικρότερο ποσοστό, στη σκληρότητα του νερού σου.

|